Lääkehoitoja uusia viruksia vastaan voidaan kehittää hyödyntämällä sekä PIKfyve- että PIP4K2C-lipidikinaaseja samanaikaisesti estäviä lääkeaineita. Kyseinen mekanismi on myös perinteisiä lääkehoitoja tehokkaampi tapa ehkäistä virusten lääkeresistenssiä.
Tuoreessa kansainvälisessä yhteistutkimuksessa kehitettiin uusia molekyyleja, joiden avulla on mahdollista estää samanaikaisesti sekä PIKfyve- että PIP4K2C-lipidikinaasien toimintaa. Lähestymistapaa pidetään lupaavana uusien virusten torjunnassa. Tutkimuksen tulokset on julkaistu Nature Communications -lehdessä ja siihen osallistui tutkijoita myös Itä-Suomen yliopistosta.
Proteiinikinaasit ovat entsyymejä, jotka katalysoivat fosfaatin siirtoa adenosiinitrifosfaatista (ATP) tyrosiini-, treoniini- tai seriiniaminohappoihin kohdeproteiineissa. Nämä fosforylaatiot ovat osa lähes jokaista solun signalointireittiä ja tarjoavat mahdollisuuksia uusille lääkevaikutuksille. Kinaaseja onkin hyödynnetty menestyksekkäästi lääkeainekohteina jo noin 30 vuoden ajan, ja markkinoille on hyväksytty lähes 90 kinaasiestäjää pääasiassa syöpien ja tulehdussairauksien hoitoon.
– Kinaasiestäjä RMC-113:n löytäminen ja hyödyntäminen edustaa merkittävää edistysaskelta isäntäsoluun kohdistuvien lipidikinaasireittien ymmärtämisessä. Kansainvälisen yhteistyön kautta olemme pystyneet vastaamaan kysymyksiin, joihin emme olisi yksin pystyneet, kertoo vanhempi tutkija Christopher Asquith Itä-Suomen yliopiston farmasian laitokselta.
Isäntäsoluun kohdistuvat hoitostrategiat, joissa kohteena ovat kinaasit, ovat houkuttelevia, koska niihin kehittyy harvemmin vastustuskyky kuin suoraan viruksiin kohdistuviin lääkkeisiin. Lisäksi lääkkeen kohdentaminen isäntäsoluun mahdollistaa tehon useampia eri viruksia vastaan, sillä monet virukset hyödyntävät samoja solureittejä lisääntyäkseen. Etsiessään laajakirjoisia viruslääkkeitä tutkijat löysivät RMC-113-nimisen molekyylin, joka estää tehokkaasti useiden RNA-virusten, kuten SARS-CoV-2:n, lisääntymistä ihmisen keuhkojen solumallissa.
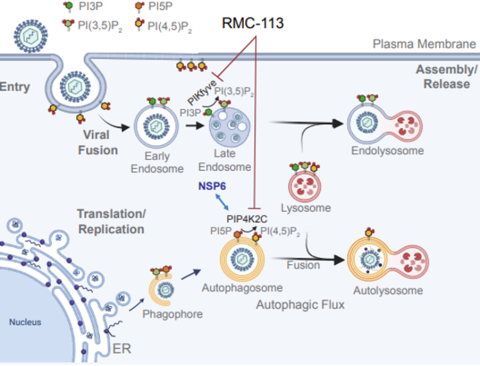
Tutkijat osoittivat, että RMC-113 ja sen läheiset analogit estävät valikoivasti lipidikinaasien PIP4K2C ja PIKfyve toimintaa. Kehittyneet lipidomiikka-analyysit paljastivat, että RMC-113 muuttaa SARS-CoV-2:n aiheuttamaa fosfoinositidiprofiilia, mikä vahvisti sen viruksia torjuvan vaikutuksen liittyvän PIP4K2C:n ja PIKfyven toiminnan estoon. Lisäksi tutkijat havaitsivat, että PIP4K2C:llä on vaikutus SARS-CoV-2-viruksen soluun pääsyssä, RNA:n replikaatiossa sekä viruksen kokoamisessa ja poistumisessa solusta, mikä vahvistaa sen soveltuvuuden lääkeainekohteeksi.
Yhdistämällä proteomiikkaa, yksittäisten solujen transkriptomiikkaa ja toiminnallisia kokeita pystyttiin osoittamaan, että PIP4K2C sitoutuu SARS-CoV-2:n ei-rakenteelliseen proteiiniin 6 ja säätelee viruksen aiheuttamaa autofagian häiriötä. Tämä autofagian normalisoiminen onkin yksi RMC-113:n viruksia torjuvan vaikutuksen mekanismeista. Tulokset osoittavat, että viruksen aikaansaama autofagian säätely PIP4K2C:n kautta on merkittävä ilmiö, ja että PIP4K2C:n ja PIKfyven toiminnan samanaikainen estäminen on lupaava strategia uusien virusten torjunnassa.
Tutkimus toteutettiin Itä-Suomen yliopiston, Stanfordin yliopiston, KU Leuven-yliopiston, Pohjois-Carolinan yliopiston Chapel Hillissä, Kööpenhaminan yliopiston, Massachusetts-Lowellin yliopiston, UNSW Sydneyn sekä Yhdysvaltain armeijan tartuntatautien tutkimuslaitoksen välisenä yhteistyönä.
Tutkimusartikkeli:
Karim M, Mishra M, Lo CW, Saul S, Cagirici HB, Gourdelier M, Ghita L, Ojha A, Tran DHN, Agrawal A, McGraw C, East MP, Gammeltoft KA, Sahoo MK, Mooney NA, Johnson GL, Das S, Leyssen P, Neyts J, Chiu W, Cohen CA, Bukh J, Gottwein J, Dye JM, Neff N, Jackson PK, Pinsky BA, Laitinen T, Pantsar T, Poso A, Zanini F, De Jonghe S, Asquith CRM, Einav S. PIP4K2C inhibition reverses autophagic flux impairment induced by SARS-CoV-2. Nat Commun. 2025, 16, 6397. doi: 10.1038/s41467-025-61759-1.